- HOME
- 製品・サービス
- 酵素法による食品分析試薬 F-キット
- F-キットのアプリケーションノート
- 第2回 酵素はどんなものか(その2)-2/2
第2回 酵素はどんなものか(その2)-2/2
第2回 酵素はどんなものか(その2) page2
4.酵素と補酵素、補助因子
ご存知のように酵素はたんぱく質でできています。
しかし酵素分子の中にはしばしばたんぱく質以外の低分子物質を含んでいます。
これらの低分子を補助因子(または補欠分子族、コファクター、など)といい、
酵素が働くときに道具として使われています。
われわれが作業をする際、布を切るのに鋏を使い、魚を取るのに釣竿を使うように、
それぞれの酵素作用に適した補助因子が必要とされます。
補助因子としては大別して①補酵素と②金属イオンがあります。
補酵素と酵素本体のたんぱく質との結合は共有結合ではなくゆるやかな結合で、
多くの場合透析やゲルろ過などで分離することが出来ます。
| 補酵素 | 関与する主な反応 | 生成元となるビタミン |
|---|---|---|
| ビオシチン | カルボキシ基化 | ビオチン |
| コバミド補酵素 | アルキル化、など | コバラミン(B12) |
| テトラヒドロ葉酸 | 炭酸基転移 | 葉酸 |
| FAD、FMN | 酸化還元 | リボフラビン(B2) |
| チアミンピロリン酸 | アルデヒド転移、脱炭酸 | チアミン(B1) |
| ピリドキサルリン酸 | アミノ基転移、ラセミ化、脱炭酸、など | ピリドキシン(B6) |
| NAD、NADP | 酸化還元 | ニコチンアミド、ナイアシン |
| コエンザイムA | アシル基転移 | パントテン酸 |
表1:補酵素とビタミン
補酵素としては約10種類が知られており、表1 にそれぞれの補酵素を道具として必要とする主な酵素反応を示しました。
表からもわかるように、補酵素を必要とするのは酸化還元作用や、化学基の転移などを触媒する酵素です。
加水分解反応をする酵素などは補酵素を必要とはしません。
また注目すべき点は、これらの補酵素はB群のビタミンから出来ていることです。
食物から取り入れられたB群のビタミンが体の中で修飾を受けて補酵素に変わるのです。
一例をあげると、欠乏すると脚気を引き起こすビタミンB1(化合物名:チアミン)は、
体内に入るとリン酸化を受けて補酵素のチアミンピロリン酸(TPP)に変わります。
TPPは糖分を燃やしてエネルギーを作る代謝にかかわる重要な酵素であるトランスケトラーゼや、
ピルビン酸脱水素酵素などの補酵素として重要な働きをします。
食物中のビタミンが欠乏すると生体に欠乏症状を引き起こすことにからみても補酵素が生体内の反応で
重要な働きをしていることがわかりますね。
ここで最も代表的な補酵素としてNAD+とNADP+について触れておきます。
この二つは酵素法による食品分析ではとりわけ重要な物質です。
これらの働きは酸化還元反応においてH+の受け渡しをします。
これらの構造はニコチンアデニンジヌクレオチドの名前が表すように図5の構造をしています。
(NADP+はNAD+に単にリン酸残基が1つ付いたもの。)
NAD+はH+を2 つ受け取ってNADHになり、逆にNADHはH+を放出してNAD+に戻りますが、
H+の入る部位はニコチン残基にあり、その部分の構造が図5の下のように変化することになります。
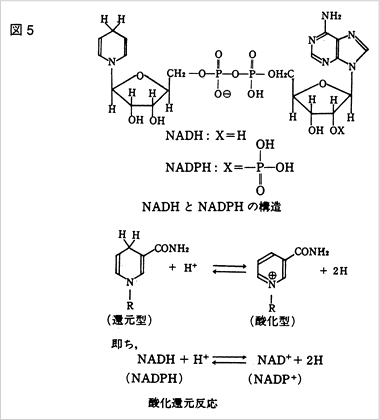
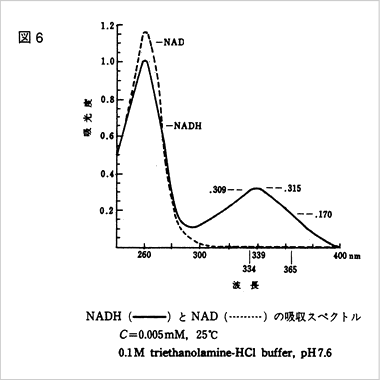
重要なことは、この構造変化に伴って光の吸収スペクトルが図6のように変化することです。
酸化型(NAD+)では340nm付近に吸収がないのに還元型(NADH)では吸収が現れます。
この性質を利用してNADH(またはNADPH)を含む酵素反応液の340 nmでの吸光度を測定することにより、
反応の度合いを知ることができ、吸光度が増加すれば還元反応量を、減少すれば酸化反応量を、
簡単かつ正確に算出できます。
金属イオンとしては、マグネシウム(Mg++)、マンガン(Mn++)、亜鉛(Zn++)、カルシウム(Ca++)、
銅(Cu++)、鉄(Fe)などが酵素分子に取り込まれ、触媒作用に直接関与しています。
補酵素の場合は、もっぱら酸化還元酵素や化学基の転移酵素に必要とされるのに対して、
金属イオンは加水分解酵素を含め、広い範囲の酵素の補助因子として働いています。
例を挙げれば、アルコールデヒドロゲナーゼやカルボキシペプチダーゼAは亜鉛を、
ATPアーゼはマグネシウムを、チロシナーゼは銅、タカアミラーゼはカルシウムを
それぞれ必要とします。
しかし金属イオンの種類と酵素の反応の種類との間にははっきりした規則性はありません。
逆に重金属イオンは微量でも酵素の活性を阻害することも多いので、酵素を取り扱うときには不要な金属イオンが
混入しないよう注意が必要です。
重金属イオンの影響を受けやすいか否かは酵素の種類によって差がありますが、
一般的には酵素が金属製の容器や器具に触れることのないよう、酵素の取扱者は十分に注意します。
酵素を精製する時などは、使用する精製水の水質に注意するのは勿論ですが、金属イオンを遮蔽する目的で
EDTAなどの金属キレート剤を緩衝液中に予防的に加えることもよく行われます。
執筆者:深見 博一(理学博士)
本書で引用した図表の出典
本文で引用した図表の出典
図1:D. E. Metzler, Biochemistry, Academic Press Inc., 1977
図2:R. K. Murray et al., Harper’s Biochemistry 21st ed., Appleton & Lange, 1988
図4:藤本大三郎, 酵素反応のしくみ, (株)講談社ブルーバックス, 2001. 12. 01.
資料ダウンロード
上記の内容をPDFでダウンロードできます。
|